В зависимости от условий тела могут находиться в жидком, твердом или газообразном состоянии. Эти состояния называются агрегатными состояниями вещества .
В газах расстояние между молекулами много больше размеров молекул. Если газу не мешают стенки сосуда, его молекулы разлетаются.
В жидкостях и твердых телах молекулы расположены ближе друг к другу и поэтому не могут удаляться далеко друг от друга.
Переход из одного агрегатного состояния в другое называется фазовым переходом .
Переход вещества из твердого состояния в жидкое называется плавлением , а температуру, при которой это происходит, – температурой плавления . Переход вещества из жидкого состояния в твердое называется кристаллизацией , а температуру перехода – температурой кристаллизации .
Количество теплоты, которое выделяется при кристаллизации тела либо поглощается телом при плавлении, отнесенное к единице массы тела, называется удельной теплотой плавления (кристаллизации) λ:
При кристаллизации выделяется такое же количество теплоты, какое поглощается при плавлении.
Переход вещества из жидкого состояния в газообразное называется парообразованием . Переход вещества из газообразного состояния в жидкое называется конденсацией . Количество теплоты, необходимое для парообразования (выделяющееся при конденсации):
| Q = Lm , |
Парообразование, происходящее с поверхности жидкости, называется испарением . Испарение может происходить при любой температуре. Переход жидкости в пар, происходящий по всему объему тела, называется кипением , а температуру, при которой жидкость кипит, – температурой кипения .
Наконец, сублимация – это переход вещества из твердого состояния непосредственно в газообразное, минуя жидкую стадию.
Если прочие параметры внешней среды (в частности, давление) остаются постоянными, то температура тела в процессе плавления (кристаллизации) и кипения не изменяется.
Если количество молекул, покидающих жидкость, равно количеству молекул, возвращающихся в жидкость, то говорят, что наступило динамическое равновесие между жидкостью и ее паром. Пар, находящийся в динамическом равновесии со своей жидкостью, называется
Любое вещество при определенных условиях может находиться в различных агрегатных состояниях – твердом, жидком и газообразном.
Область, в которой вещество однородно по всем физическим и химическим свойствам, называется фазой состояния этого вещества.
Переход из одного состояния в другое называется фазовым переходом .
Фазовый переход происходит при изменении температуры тела, т.е. при фазовом переходе изменяется внутренняя энергия вещества.
Одним из важнейших понятий термодинамики является внутренняя энергия тела. Все макроскопические тела обладают энергией, заключенной внутри самих тел. С точки зрения молекулярно-кинетической теории внутренняя энергия вещества складывается из кинетической энергии всех атомов и молекул и потенциальной энергии их взаимодействия друг с другом .
Внутренняя энергия – это сумма энергий молекулярных взаимодействий и энергии теплового движения молекул.
В частности, внутренняя энергия идеального газа равна сумме кинетических энергий всех частиц газа, находящихся в непрерывном и беспорядочном тепловом движении. Внутренняя энергия идеального газа зависит только от его температуры и не зависит от объема (закон Джоуля).
Внутреннюю энергию тела можно изменить разными способами :
- Совершение механической работы.
- Теплообмен.

Количеством теплоты Q , полученной телом, называют изменение внутренней энергии тела в результате теплообмена.
Количество теплоты Q является энергетической величиной. В СИ количество теплоты измеряется в единицах механической работы – джоулях (Дж).
Если в результате теплообмена телу передается некоторое количество теплоты, то внутренняя энергия тела и его температура изменяются.
Чтобы нагреть тело массой m от температуры t 1 до температуры t 2 ему необходимо сообщить количество теплоты
Q = cm (t 2 – t 1 )
Количество теплоты Q, необходимое для нагревания 1 кг вещества на 1 К называют удельной теплоемкостью вещества c.
c = Q / (mΔT).
Испарение и конденсация являются примерами фазовых переходов.
Все реальные газы (кислород, азот, водород и т. д.) при определенных условиях способны превращаться в жидкость.
Переход вещества из жидкого состояния в газообразное называется парообразованием.
Парообразование, происходящее со свободной поверхности жидкости называется испарением.
С точки зрения молекулярно-кинетической теории, испарение – это процесс, при котором с поверхности жидкости вылетают наиболее быстрые молекулы, кинетическая энергия которых превышает энергию их связи с остальными молекулами жидкости. Это приводит к уменьшению средней кинетической энергии оставшихся молекул, то есть к охлаждению жидкости (если нет подвода энергии от окружающих тел). Жидкость при испарении охлаждается (ощущение холода при выходе из воды).

Покинувшие жидкость молекулы составляют пар над её поверхностью. Некоторые молекулы пара при хаотическом движении над поверхностью жидкости залетают обратно в жидкость. Это означает, что наряду с испарением жидкости всегда происходит и конденсация её паров. При конденсации молекулы пара возвращаются в жидкость.
Конденсация – это процесс превращения пара в жидкость.
Скорость испарения зависит:
- от рода жидкости (эфир и вода);
- от площади её свободной поверхности (чем больше площадь, тем быстрее испаряется жидкость – блюдце и стакан);
- от температуры (чем выше температура, тем быстрее испаряется жидкость – лужи зимой и летом);
- от наличия движения воздуха над поверхностью (в ветреную погоду и в безветренную).
На практике для превращения жидкости в пар в процессе теплообмена к ней подводится теплота.
Количество теплоты Q п, необходимое для превращения жидкости в пар при неизменной температуре называется теплотой парообразования.
Для того, чтобы превратить в пар при неизменной температуре жидкость массой m , ей необходимо сообщить количество теплоты, равное Q п = r·m
r – удельная теплота парообразования – количество теплоты, необходимое для превращения в пар 1 кг жидкости при неизменной температуре [Дж/кг]
При конденсации выделяется количество теплоты, равное Q к = - r·m
Испарение может происходить не только с поверхности, но и в объеме жидкости.
В жидкости всегда имеются мельчайшие пузырьки газа. Если давление насыщенного пара жидкости равно внешнему давлению (то есть давлению газа в пузырьках) или превышает его, жидкость будет испаряться внутрь пузырьков. Пузырьки, наполненные паром, расширяются и всплывают на поверхность. Этот процесс называется кипением .

Кипением называют парообразование, которое происходит в объеме всей жидкости при постоянной температуре.
Кипение жидкости начинается при такой температуре, при которой давление ее насыщенных паров становится равным внешнему давлению .
Каждая жидкость при нормальных условиях кипит при определенной температуре, которая называется температура кипения. Она остается постоянной при одном и том же давлении.
Вещество существует в твердом кристаллическом состоянии при определенных значениях давления и температуры. В этом состоянии вещество находится до тех пор, пока кинетической энергии атомов недостаточно, чтобы преодолеть силы взаимного притяжения. Эти силы удерживают атомы на некотором расстоянии друг относительно друга, не позволяя им перемещаться. При этом атом колеблется около положения своего равновесия. При нагревании твердого тела кинетическая энергия атомов или молекул возрастает. При этом амплитуды колебаний могут стать настолько большими, что уже будут сравнимы с периодом решетки, произойдет нарушение дальнего порядка, кристаллическая решетка начнет разрушаться. При дальнейшем увеличении температуры происходит плавление твердых тел.
Плавление – переход вещества из твердого состояния в жидкое.
При плавлении температура тела остается постоянной . Все переданное телу тепло идет на разрушение кристалла. При плавлении кристаллическое тело находится одновременно в твердом и жидком состояниях.
После разрушения кристалла и образования жидкости подводимая теплота идет на нагревание жидкости.
Температура плавления зависит от рода кристаллического тела.
При плавлении изменяется плотность и объем вещества. У большинства веществ объем при плавлении увеличивается, а при отвердевании уменьшается. При этом изменяется и плотность: при плавлении плотность уменьшается, а при отвердевании увеличивается. Например, кристаллики твердого нафталина или парафина тонут в расплавленном нафталине (парафине).
Но лед плавает в воде. Также ведут себя висмут, галлий, германий, кремний, чугун, т.е. при плавлении их плотность увеличивается, а при отвердевании уменьшается. При плавлении они сжимаются (объем уменьшается), а при отвердевании расширяются (объем увеличивается).
Температура плавления зависит от атмосферного давления.
В тех случаях, когда объем вещества при плавлении возрастает, увеличение внешнего давления приводит к увеличению температуры плавления (т.к. увеличение давления затрудняет процесс плавления). Если же объем вещества при плавлении уменьшается, то увеличение внешнего давления ведет к понижению температуры плавления этого вещества (т.к. повышенное давление помогает процессу плавления в данном случае).
Чтобы перевести в жидкость твердое тело массой m при температуре плавления, ему надо сообщить количество теплоты
Q = λ m
где λ – удельная теплота плавления – количество теплоты, необходимое, чтобы перевести в жидкость твердое тело массой 1 кг при температуре плавления.
λ = Q / m [ Дж/кг ]
При плавлении увеличивается внутренняя энергия тела.
Если получившуюся при плавлении жидкость охладить до температуры плавления, то начнется обратный процесс.
Кристаллизация (отвердевание) – процесс перехода жидкости в твердое состояние.
Происходит сближение частиц жидкости и упорядочение их движения, в результате которого они начинают колебаться около узлов кристаллической решетки. Потенциальная энергия молекул при этом уменьшается, а т.к. температура кристаллизации постоянна (равна температуре плавления для данного вещества), процесс кристаллизации должен сопровождаться выделением тепла.
Процесс кристаллизации сопровождается выделением теплоты кристаллизации, которая равна теплоте плавления Q = λ m
Процесс кристаллизации происходит в двухфазной системе вблизи центров кристаллизации. такими центрами могут быть пылинки, мельчайшие примеси.
Процессы плавления и кристаллизации можно представить на графике:

По графику можно определить:

- участок АВ – нагревание льда от -40 0 С до температуры плавления 0 0 С
- участок ВС – плавление льда при температуре плавления
- участок СD – нагревание воды от 0 0 С до температуры 50 0 С
- участок DE – охлаждение воды от 50 0 С до температуры кристаллизации (отвердевания) 0 0 С
- участок EF – кристаллизация (отвердевание) воды при температуре плавления (кристаллизации)
- участок FK – охлаждение льда от 0 0 С до температуры -40 0 С
Многие твердые вещества обладают запахом – камфара, нафталин. Значит пары этих веществ есть в воздухе. Это доказывает, что при определенных условиях твердые вещества могут переходить из твердого состояния в газообразное, минуя жидкое.
Переход твердого состояния вещества в газообразное называется сублимацией или возгонкой («сублимаре» - возносить)
Легко обнаружить возгонку (сублимацию) льда и снега: уменьшение инея на деревьях со временем, высыхание оледеневшего белья зимой.
Часто можно наблюдать и обратный переход из газообразного состояния непосредственно в твердое, минуя жидкое состояние – десублимация. На окнах зимой иногда можно видеть быстрый рост кристалликов льда в виде узоров на стеклах, которые образуются непосредственно из водяных паров, находящихся в воздухе.
Испарение твердых тел аналогично испарению жидкостей. Все твердые тела испаряются, но их паров обычно так мало, что их невозможно обнаружить. Процесс сублимации происходит как при нагревании твердого тела, так и без подвода теплоты извне. При сублимации происходит охлаждение тела, т.к. его покидают наиболее быстрые молекулы (обладающие кинетической энергией, достаточной для преодоления молекулярного притяжения и отрыва молекул от поверхности тела).
Процесс сублимации или возгонки наблюдается во Вселенной. При сближении с солнцем происходит возгонка поверхностного слоя ядер комет. Практически вся масса кометы сосредоточена в ядре, которое является единственной твердой частью кометы. Ядро кометы состоит из смеси пылинок, твердых кусочков вещества и замерзших газов (углекислый газ, аммиак, метан). В далеких от Солнца областях кометы не имеют хвостов. При приближении кометы к Солнцу ядро прогревается и из него выделяются газы и пыль. Они образуют вокруг ядра газовую оболочку, которая вместе с ядром составляет голову кометы. Газы и пыль, выбрасываемые в голову кометы, отталкиваются под действия давления солнечного света и создают хвост кометы, всегда направленный в сторону, противоположную Солнцу. Чем ближе к Солнцу подходит комета, тем она ярче и тем длиннее её хвост вследствие большего её облучения и интенсивного выделения газов.
В окружающем нас мире постоянно и непрерывно происходит огромное множество различных физических явлений и процессов. Одним из немаловажных можно считать процесс испарения. Существует несколько обязательных условий для данного явления. В этой статье мы разберем каждый из них более подробно.
Это процесс преобразования веществ в газообразное или парообразное состояние. Оно характерно только для консистенции. Однако нечто похожее наблюдается и у твердых тел, только называется данное явление сублимацией. Это можно заметить при тщательном наблюдении за телами. Например, кусок мыла с течением времени подсыхает и начинает трескаться, это объясняется тем, что капельки воды в его составе испаряются и переходят в газообразное состояние H 2 O.
Определение в физике
Испарение - это эндотермический процесс, при котором источником поглощаемой энергии служит теплота Она включает в себя две составляющие:
- определенное необходимое для преодоления молекулярных сил притяжения, когда происходит разрыв между соединенными молекулами;
- теплота, необходимая при работе расширения молекул в процессе превращения жидких веществ в пар или газ.

Как это происходит?
Переход вещества из жидкого состояния в газообразное может происходить двумя способами:
- Испарение - это процесс, при котором с поверхности жидкого вещества улетучиваются молекулы.
- Кипение - процесс парообразования из жидкости путем доведения температуры до удельной теплоты кипения вещества.
Несмотря на то что оба эти явления преобразуют жидкое вещество в газ, между ними есть существенные различия. Кипение - это активный процесс, который совершается только при определенной температуре, тогда как испарение происходит при любых условиях. Еще одно отличие заключается в том, что кипение характерно для всей толщи жидкости, а второе явление возникает только на поверхности жидких веществ.
Молекулярно-кинетическая теория испарения
Если рассматривать данный процесс на молекулярном уровне, то он происходит следующим образом:
- Молекулы в жидких веществах находятся в постоянном хаотичном движении, все они имеют абсолютно разные скорости. Между тем частицы притягиваются друг к другу благодаря силам притяжения. Каждый раз когда они сталкиваются друг с другом, их скорости меняются. В какой-то момент у некоторых развивается очень большая скорость, позволяющая преодолеть силы притяжения.
- Эти элементы, которые оказались на поверхности жидкости, обладают такой кинетической энергией, что способны преодолевать межмолекулярные связи и покидать жидкость.
- Именно эти самые быстрые молекулы вылетают с поверхности жидкого вещества, причем происходит этот процесс постоянно и непрерывно.
- Оказавшись в воздухе, они превращаются в пар - называется это парообразованием.
- Как следствие этого, оставшихся частиц становится все меньше. Этим и объясняется остывание жидкости. Вспомните, как в детстве нас учили дуть на горячую жидкость, чтобы она скорее остыла. Получается, что мы ускоряли процесс и спад температуры происходил намного быстрее.

От каких факторов зависит?
Существует множество условий, необходимых для возникновения данного процесса. Оно происходит отовсюду, где присутствуют частицы воды: это и озера, моря, реки, все влажные предметы, покровы тел животных и людей, а также листья растений. Можно сделать вывод, что испарение - это весьма значимый и незаменимый процесс для окружающего мира и всех живых существ.
Вот какие факторы оказывают влияние на данное явление:
- Скорость испарения напрямую зависит от состава самой жидкости. Известно, что у каждой из них существуют свои особенности. Например, те вещества, у которых теплота парообразования ниже, будут преобразовываться быстрее. Сравним два процесса: испарение спирта и обычной воды. В первом случае преобразование в газообразное состояние происходит быстрее, потому что удельная теплота парообразования и конденсации у спирта равна 837 кДж/кг, а у воды почти в три раза больше - 2260 кДж/кг.
- Скорость также зависит от изначальной температуры жидкости: чем она больше, тем быстрее образуется пар. В качестве примера возьмем стакан воды, когда внутри сосуда находится кипяток, то парообразование происходит с гораздо большей скоростью, нежели когда температура воды ниже.
- Еще один фактор, определяющий скорость протекания данного процесса, - это площадь поверхности жидкости. Вспомните, что в тарелке большого диаметра горячий суп остывает быстрее, чем в маленьком блюдце.
- Скорость распространения веществ в воздушной среде во многом определяет и скорость испарения, т. е. чем быстрее происходит диффузия, тем скорее происходит парообразование. Например, при сильных ветрах капельки воды быстрее испаряются с поверхности озер, рек и водохранилищ.
- Температура воздуха в помещении также играет немаловажную роль. Подробнее об этом мы поговорим чуть ниже.

Какова роль влажности воздуха?
Вследствие того что процесс испарения происходит отовсюду непрерывно и постоянно, то в воздухе всегда присутствуют частички воды. В молекулярном виде они выглядят как группа элементов H 2 O. Жидкости могут испаряться в зависимости от показателя объема водяных паров в атмосфере, этот коэффициент и называется влажностью воздуха. Она бывает двух видов:
- Относительная влажность - это отношение количества водяных паров в воздухе к плотности насыщенного пара при той же температуре в процентном соотношении. Например, показатель 100 % говорит о том, что атмосфера полностью насыщена молекулами H 2 O.
- Абсолютная же характеризует плотность водяных паров в воздушной среде, обозначается буквой f и показывает, какая масса молекул воды содержится в 1м 3 воздуха.
Связь процесса испарения и влажности воздуха можно определить следующим образом. Чем меньше показатель тем быстрее будет происходить испарение с поверхности земли и других предметов.
Испарение различных веществ
У различных веществ этот процесс протекает по-разному. Например, испарение спирта происходит быстрее, чем у многих жидкостей благодаря его маленькой удельной теплоте парообразования. Зачастую подобные жидкие вещества называются летучими, потому что водяные пары буквально улетучиваются из них практически при любых температурах.

Спирт также может испаряться даже при комнатной температуре. В процессе готовки вина или водки спирт прогоняется через самогонный аппарат, только достигнув температуры кипения, она приблизительно равняется 78 градусам. Однако реальная температура испарения спирта будет немного больше, потому как в исходном продукте (например, браге) он представляет собой соединения с различными ароматическими маслами и водой.
Конденсация и сублимация
Следующее явление можно наблюдать каждый раз, когда закипает вода в чайнике. Обратите внимание, что при кипении вода переходит из жидкого состояния в газообразное. Происходит это таким образом: горячая струя водяного пара с большой скоростью вылетает из чайника через его носик. При этом образовавшийся пар виден не прямо у выхода из носика, а на небольшом расстоянии от него. Данный процесс называется конденсацией, т. е. водяные пары сгущаются до такой степени, что становятся видны для наших глаз.

Испарение твердого тела называется сублимацией. При этом они переходят из агрегатного состояния в газообразное, минуя стадию жидкости. Самый известный случай сублимации связан с кристаллами льда. В первоначальном виде лед является твердым веществом, при температуре выше 0° он начинает таять, принимая жидкое состояние. Однако в некоторых случаях при отрицательных температурах лед переходит в парообразную форму, минуя жидкую фазу.
Влияние испарения на человеческий организм
Благодаря испарению в нашем теле происходит терморегуляция. Происходит данный процесс через систему самоохлаждения. В жаркий знойный день человеку, который занимается определенным физическим трудом, становится очень жарко. Это означает, что в нем увеличивается внутренняя энергия. А как известно, при температуре выше 42° белок в крови человека начинает сворачиваться, если вовремя не остановить этот процесс, он приведет к смерти.

Система самоохлаждения устроена как раз таким образом, чтобы регулировать температуру для нормальной жизнедеятельности. Когда температура становится предельно допустимой, через поры на коже начинается активное потоотделение. А затем уже с поверхности кожи происходит испарение, которое поглощает лишнюю энергию тела. Иными словами, испарение - это процесс, способствующий охлаждению организма до нормального состояния.
Установлению идеального порядка в расположении атомов, т. е. образованию твердого тела, препятствуют тепловые движения, главной особенностью которых является, как мы знаем, хаотичность, беспорядочность. Поэтому для того, чтобы вещество могло находиться в твердом состоянии, его температура должна быть достаточно низкой - настолько низкой, чтобы энергия тепловых движений была меньше, чем потенциальная энергия взаимодействия атомов.
Вполне идеальным кристаллом, в котором все атомы находятся в равновесии и обладают минимальной энергией, тело может быть только при абсолютном нуле. В действительности все вещества становятся твердыми при значительно более высоких температурах. Исключение составляет только гелий, который остается жидким и при абсолютном нуле, но это связано с некоторыми квантовыми эффектами, о которых мы кратко скажем ниже.
В твердое состояние вещество может перейти как из жидкого, так и из газообразного состояния. И в том и в другом случае такой переход есть переход из состояния, лишенного симметрии, в состояние, в котором симметрия существует (это во всяком случае относится к дальнему порядку, существующему в кристаллах, но не существующему ни в жидких, ни в газообразных веществах). Поэтому переход в твердое состояние должен происходить скачком, т. е. при определенной температуре, в отличие от перехода газ - жидкость, который, как мы знаем, может происходить и непрерывным образом.
Рассмотрим сначала превращение жидкость-твердое тело. Процесс образования твердого тела при охлаждении жидкости есть процесс образования кристалла (кристаллизация), (и происходит он при определенной температуре температуре кристаллизации или отвердевания. Так как при таком превращении энергия уменьшается, то оно сопровождается выделением энергии в виде скрытой теплоты кристаллизации. Обратное превращение - плавление - также происходит скачком при тон же температуре и сопровождается поглощением энергии в виде
той теплоты плавления, равной по величине теплоте кристаллизации.
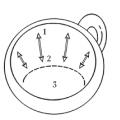
Это ясно видно из графика зависимости температуры охлаждающейся жидкости от времени, изображаемого на рис. 179 (кривая а). Участок 1 кривой а дает ход монотонного понижения температуры жидкости вследствие отвода тепла от нее. Горизонтальный участок 2 показывает, что при определенном значении температуры ее понижение прекращается, несмотря на то, что отвод тепла продолжается. Через некоторое время температура снова начинает понижаться (участок 3). Температура, соответствующая участку 2, это и есть температура кристаллизации. Выделяющееся при кристаллизации тепло компенсирует отвод тепла от вещества и поэтому понижение температуры временно прекращается. После окончания процесса кристаллизации температура, теперь уже твердого тела, вновь начинает понижаться.

Такой ход графика понижения температуры характерен для кристаллических тел. При охлаждении жидкостей, не кристаллизующихся (аморфных веществ), скрытая теплота не выделяется и график охлаждения представляет собой монотонную кривую без остановки охлаждения.
При обратном процессе перехода вещества из твердого состояния в жидкое (плавление) на кривой нагревания также наблюдается остановка в повышении температуры, вследствие поглощения скрытой теплоты плавления - теплоты, за счет которой происходит разрушение кристаллической решетки (кривая на рис. 179).
Для начала кристаллизации необходимо присутствие центра или центров кристаллизации. Такими центрами могли бы служить случайные скопления частиц жидкости, прилипших друг к другу, к которым могли бы присоединяться всё новые и новые частицы, пока вся жидкость не обратилась бы в твердое тело. Однако образование таких скоплений в самой жидкости затрудняется тепловыми движениями, которые их разрушают еще до того, как они успевают приобрести сколько-нибудь заметные размеры. Кристаллизация существенно облегчается, если в жидкости с самого начала присутствуют достаточно большие твердые частицы в виде пылинок и тел, которые становятся центрами кристаллизации.
Образование центров кристаллизации в самой жидкости облегчается, конечно, с понижениемтемпературы. Поэтому кристаллизация чистой жидкости, лишенной посторонних образований,
начинается обычно при температуре несколько более низкои, чем истинная температура кристаллизации. В обычных условиях в кристаллизующейся жидкости имеется много центров кристаллизации, так что в жидкости образуется множество кристалликов, срастающихся вместе, и затвердевшее вещество оказывается поликристаллическим.
Только в особых условиях, которые обычно трудно обеспечить, можно получить одиночный кристалл - монокристалл, вырастающий из единственного центра кристаллизации. Если при этом для всех направлений обеспечены одинаковые условия накопления частиц, то кристалл получается правильно ограненным соответственно его свойствам симметрии.
Переход жидкость - твердое тело, так же как и обратное превращение, является фазовым переходом, так как жидкое и твердое состояния можно рассматривать как две фазы вещества. Обе фазы при температуре кристаллизации (плавления) могут соприкасаться друг с другом, находясь в равновесии (лед, например, может плавать в воде, не плавясь), так же как могут находиться в равновесии жидкость и ее насыщенный пар.
Подобно тому как температура кипения зависит от давления, температура кристаллизации (и равная ей температура плавления) также зависит от давления, обычно возрастая с ростом давления. Растет она потому, что внешнее давление сближает атомы между собой, а для разрушения кристаллической решетки при плавлении атомы нужно отдалить друг от друга: при большем давлении для этого требуется большая энергия тепловых движений, т. е. более высокая температура.

На рис. 180 показана кривая зависимости температуры плавления (кристаллизации) от давления. Сплошная кривая делит всю область на две части. Область влево от кривой соответствует твердому состоянию, а область справа от кривой - жидкому состоянию. Любая же точка, лежащая на самой кривой плавления, соответствует равновесию твердой и жидкой фаз: при этих давлениях и температурах вещество в жидком и твердом состояниях находится в равновесии, соприкасаясь друг с другом, и при этом жидкость не твердеет, а твердое тело не плавится.
Пунктиром на рис. 180 показана кривая плавления для тех немногих веществ (висмут, сурьма, лед, германий), у которых при отвердевании объем не уменьшается, а увеличивается. У таких
веществ, естественно, температура плавления с повышением давления понижается.
Изменение температуры плавления связано с изменением давления соотношением Клапейрона - Клаузиуса:
![]()
Здесь - температура плавления (кристаллизации), и - соответственно молярные объемы жидкой и твердой фаз и молярная теплота плавления.
Эта формула справедлива и для других фазовых переходов. В частности, для случая испарения и конденсации формула Клапейрона-Клаузиуса была выведена в гл. VII [см. (105.6)].
Из формулы Клапейрона - Клаузиуса видно, что знак изменения температуры плавления с изменением давления определяется тем, какая из двух величин, или больше. Крутизна кривой зависит также от величины скрытой теплоты перехода чем меньше тем меньше изменяется температура плавления с давлением. В табл. 20 приведены значения удельной (т. е. отнесенной к единице массы) теплоты плавления для некоторых веществ.
Таблица 20 (см. скан) Удельная теплота плавления для некоторых веществ
Уравнение Клапейрона - Клаузиуса может быть написано и в таком виде:
![]()
Это уравнение показывает, как изменяется давление, под которым находятся обе равновесные фазы, при изменении температуры.
Твердое тело может образоваться не только путем кристаллизации жидкости, но и конденсацией газа (пара) в кристалл, минуя жидкую фазу. При этом также выделяется скрытая теплота перехода, которая, однако, всегда больше скрытой теплоты плавления. Ведь образование твердого тела при определенных температуре и давлении может произойти как непосредственно из газообразного состояния, так и путем предварительного ожижения, В обоих
случаях начальное и конечное состояния одинаковы. Одинакова, значит, и разность энергий этих состояний. Между тем во втором случае выделяется, во-первых, скрытая теплота конденсации при переходе из газообразного в жидкое состояние и, во-вторых, скрытая теплота кристаллизации при переходе из жидкого в твердое состояние. Отсюда следует, что скрытая теплота при непосредственном образовании твердого тела из газообразной фазы должна быть равна сумме теплоты конденсации и кристаллизации из жидкости. Это относится только к теплотам, измеренным при температуре плавления. При более низких температурах теплота конденсации из газа возрастает.
Обратный процесс испарения твердого тела называется обычно возгонкой или сублимацией. Испаряющиеся частицы твердого тела образуют над ним пар совершенно так же, как это происходит при испарении жидкости. При определенных давлении и температуре пар и твердое тело могут находиться в равновесии. Пар, находящийся в равновесии с твердым телом, также называется насыщенным паром. Как и в случае жидкости, упругость насыщенного пара над твердым телом зависит от температуры, быстро уменьшаясь с понижением температуры, так что у многих твердых тел при обычных температурах упругость насыщенного пара ничтожно мала.

На рис. 181 показан вид кривой зависимости упругости насыщенного пара от температуры. Эта кривая является линией равновесия твердой и газообразной фаз. Область слева от кривой соответствует твердому состоянию, справа от нее - газообразному. Возгонка, так же как и плавление, связана с разрушением решетки и требует затраты необходимой для этого энергии. Эта энергия проявляется как скрытая теплота возгонки (сублимации), равная, разумеется, скрытой теплоте конденсации.. Теплота возгонки равна поэтому сумме теплот плавления и парообразования.
Что же такое «тройная точка» и как определить её координаты? Опыты показывают, что для каждого вещества существуют условия (давление и температура), при которых пар, жидкость и кристалл могут сосуществовать одновременно сколь угодно долго. Например, если поместить в закрытый сосуд при нуле градусов воду с плавающим льдом, то в свободное пространство будут испаряться и вода, и лёд. Однако при давлении паров 0,006 атм. (это «собственное» их давление, без учёта давления, создаваемого воздухом) и температуре 0,01 °С увеличение массы пара прекратится. С этого момента лёд, вода и пар будут сохранять свои массы сколь угодно долго. Это и есть тройная точка для воды (левая диаграмма). Если в условия левой области поместить воду или пар, то они станут льдом. Если в «нижнюю область» внести жидкость или твёрдое тело, то получится пар. В правой области вода будет конденсироваться, а лёд плавиться.
Аналогичную диаграмму можно построить для любого вещества. Цель таких диаграмм – дать ответ на вопрос: какое состояние вещества будет устойчивым при таком-то давлении и такой-то температуре. Например, правая диаграмма построена для углекислого газа. Тройная точка для этого вещества имеет координату «давление» 5,11 атм, то есть значительно больше, чем нормальное атмосферное давление. Поэтому при обычных условиях (давление 1 атм) мы можем наблюдать только переходы «ниже тройной точки», то есть самостоятельное превращение твёрдого тела в газ. При давлении 1 атм это будет происходить при температуре –78 °С (см. пунктирные линии координат ниже тройной точки).
Все мы живём «около» значений «нормальных условий», т. е. прежде всего при давлении, близком к одной атмосфере. Поэтому, если атмосферное давление, ниже давления, соответствующего тройной точке, при нагревании тела мы не увидим жидкости, – твёрдое вещество будет превращаться сразу в пар. Именно так и ведёт себя «сухой лёд», что очень удобно для продавцов мороженого. Брикеты мороженого можно перекладывать кусками «сухого льда» и не бояться при этом, что мороженое намокнет. Если же давление, соответствующее тройной точке, меньше атмосферного, то вещество относится к «плавящимся» – при повышении температуры оно сначала превращается в жидкость, а потом закипает.
Как видите, особенности агрегатных превращений веществ напрямую зависят от того, как текущие значения давления и температуры соотносятся с координатами «тройной точки» на диаграмме «давление-температура».
И в заключение назовём известные вам вещества, всегда сублимирующие при нормальных условиях. Это йод, графит, «сухой лёд». При давлениях и температурах, отличных от нормальных, эти вещества вполне можно наблюдать и в жидком, и даже в кипящем состоянии.
(C) 2013. Физика.ru при участии А.В.Кузнецовой (г. Самара)